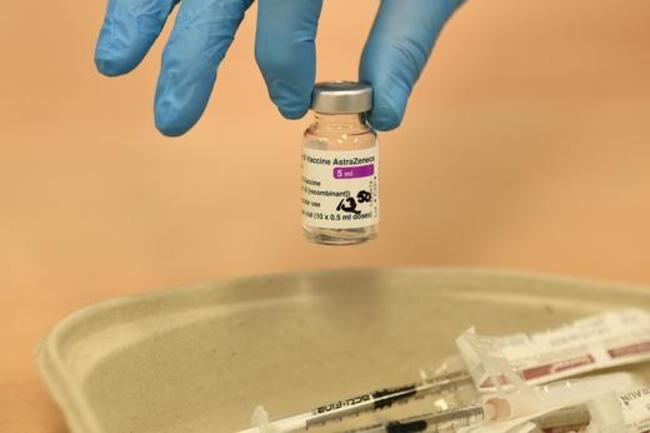
Jakarta, Gatra.com – Pandemi belum usai. Akan tetapi, harapan mengenai kembalinya kehidupan ke situasi normal kian meninggi mengingat program vaksinasi sedang berjalan. Sejauh ini tujuh vaksin yang akan beredar di Indonesia. Sesuai dengan keputusan Menteri Kesehatan, tujuh vaksin tersebut adalah Sinovac, Biofarma, Sinopharm, AstraZeneca, Pfizer, Moderna, dan Novavax. Hanya saja, informasi mengenai izin peredaran, kemanjuran, dan keamanan vaksin-vaksin tersebut dinilai masih minim.
Direktur Registrasi Obat dari Badan Pengawas Obat dan Makanan (BPOM), Rizka Andalusia, memaparkan persoalan ini dalam sebuah program talkshow virtual Bibir Covid (Bincang-bincang Seputar Covid-19) seri ke-XXVII yang bertajuk “Mengenal Pelbagai Jenis Vaksin Covid-19 yang Akan Beredar di Indonesia” yang digelar secara daring Kamis, (1/4).
Menurut keterangan Rizka, sejauh ini terdapat tiga jenis vaksin yang sudah disetujui oleh BPOM untuk digunakan dalam program vaksinasi di Indonesia. Vaksin-vaksin tersebut adalah Sinovac, Biofarma, dan AstraZeneca.
Vaksin Sinovac diimpor langsung dari Sinovac Beijing. Sementara Biofarma adalah vaksin yang proses fill and finish-nya dilakukan di Biofarma tapi bahan bakunya berasal dari Sinovac Beijing. Lalu, vaksin AstraZeneca diperoleh dari Korea Selatan melalui mekanisme COVAX facility.
Rizka menyebut bahwa vaksin-vaksin ini bisa digunakan dalam program vaksinasi dengan Izin Penerbitan Darurat. “Tentunya semua vaksin yang akan digunakan dalam program vaksinasi sesuai dengan Perpres harus mendapatkan izin penggunaan dalam kondisi darurat atau yang kita kenal dengan nama Emergency Use Authorization dari Badan POM,” ujarnya.
“Makna dari pemberian Emergency Use Authorization ini (maksudnya adalah) telah dilakukan evaluasi bersama Badan POM terkait ketiga aspek yang menjadi persyaratan untuk mendapatkan izin penggunaan, yaitu khasiat, keamanan dan mutu,” tambahnya.
Menurut Rizka, evaluasi terhadap data-data mengenai khasiat dan keamanan vaksin dilaksanakan berdasarkan data-data klinis yang telah dilakukan oleh pengembang vaksin yang diserahkan kepada BPOM. Setelah itu, BPOM bisa melakukan evaluasi mengenai tingkat keamanannya.
“Yang pertama keamanan dulu dan yang berikutnya adalah khasiatnya. Sesuai dengan standar WHO, WHO mensyaratkan minimal efikasi vaksin yang dapat digunakan dalam penanganan Covid-19 ini adalah 50% efikasinya. Jadi kalau sudah di atas 50% kita bisa terima,” terang Rizka.
Selain tingkat keamanan, BPOM juga menaruh perhatian pada mutu vaksin. “Badan POM mempunyai berbagai kriteria mutu dari vaksin yang harus dipenuhi oleh pendaftar vaksin tersebut. Karena bagaimana pun juga bagusnya (atau) khasiatnya suatu vaksin, dan dari uji kliniknya dinyatakan aman, tapi manakala mutunya tidak bisa dijamin atau tidak baik, maka akan berpengaruh terhadap keamanan,” jelas Rizka.
“Dengan mengevaluasi khasiat, keamanan, dan mutu tersebut, dapat dinyatakan bahwa vaksin tersebut sudah aman dan berkhasiat untuk digunakan dalam program vaksinasi,” pungkasnya.





_thumb.jpg)











_(1)_11zon1_thumb.jpg)















